RNAi治療薬の仕組み
RNAiを用いた私たちの治療薬は、疾患の原因となる特定の遺伝子を“沈黙”させることで、タンパク質の合成を抑制します。
RNAiは、DNAの新しいタンパク質を作る命令を伝える役割を持つメッセンジャーRNA(mRNA)に “干渉” することによって、遺伝 ⼦発現(タンパク質の合成)を制御する生物にもともと備わっている自然なプロセスです。当社のRNAi治療薬は、このプロセスを再現し、特別に設 計された低分⼦⼲渉RNA(small interfering RNA: siRNA)を送達することで、RNA誘導サイレンシング複合体(RISC: RNA-induced silencing complex)の⼀部として、疾患の原因となる特定のmRNAに結合し、ハサミのようにその分解を誘導し、疾患の原因と なるタンパク質の産⽣を抑制します。
遺伝学的に検証された標的に作⽤することで、当社のRNAi治療薬は、低分⼦化合物やモノクローナル抗体など、他の多く の医薬品よりも “上流” で作⽤します.
mRNAとsiRNAの役割
遺伝子発現とは、DNAに書かれた一連の情報がタンパク質に変換されるプロセスのことです。タンパク質は、生命活動の「担い手」であり、ほとんどすべての身体機能に関与しています。組織の生成や修復、脳、心臓、肺、肝臓、骨、筋肉、軟骨、血液、皮膚の発達に不可欠であり、体内で働く酵素やホルモンなど多くの化学物質を構成しています。DNA内のタンパク質の情報をもとにmRNAが合成され、そのmRNAが核から細胞質へと運ばれ、そこでリボソームによって新しいタンパク質が作られます。
時に、“変異”と呼ばれるDNA内のエラーが起こり、病気の原因となるタンパク質を合成する異常なmRNAを生み出すことがあります。このような場合、 アルナイラムのRNAi治療アプローチは、siRNAを利用して特定のmRNAを標的にして分解することで治療を行います。その他にsiRNAを用いた例としては、疾患に関与しない他のタンパク質(単一の遺伝子変異によるものではない)を標的とし、そのタンパク質の合成を抑制することによって治療効果をもたらすことも可能です。このアプローチにより、RNAi治療薬は、脂質異常症や高血圧症など、より広範な疾患に対応することが可能となります。
私たちは、ゲノム上のあらゆる遺伝⼦を標的とするsiRNAの設計ができると信じています
当社のsiRNAを合成する能⼒と、RNAi治療薬の⾼い再現性とモジュール化する技術を特徴とする研究開発体制が、希少疾患から ⼀般的な疾患まで幅広い疾患に対応できる可能性を切り開きます.
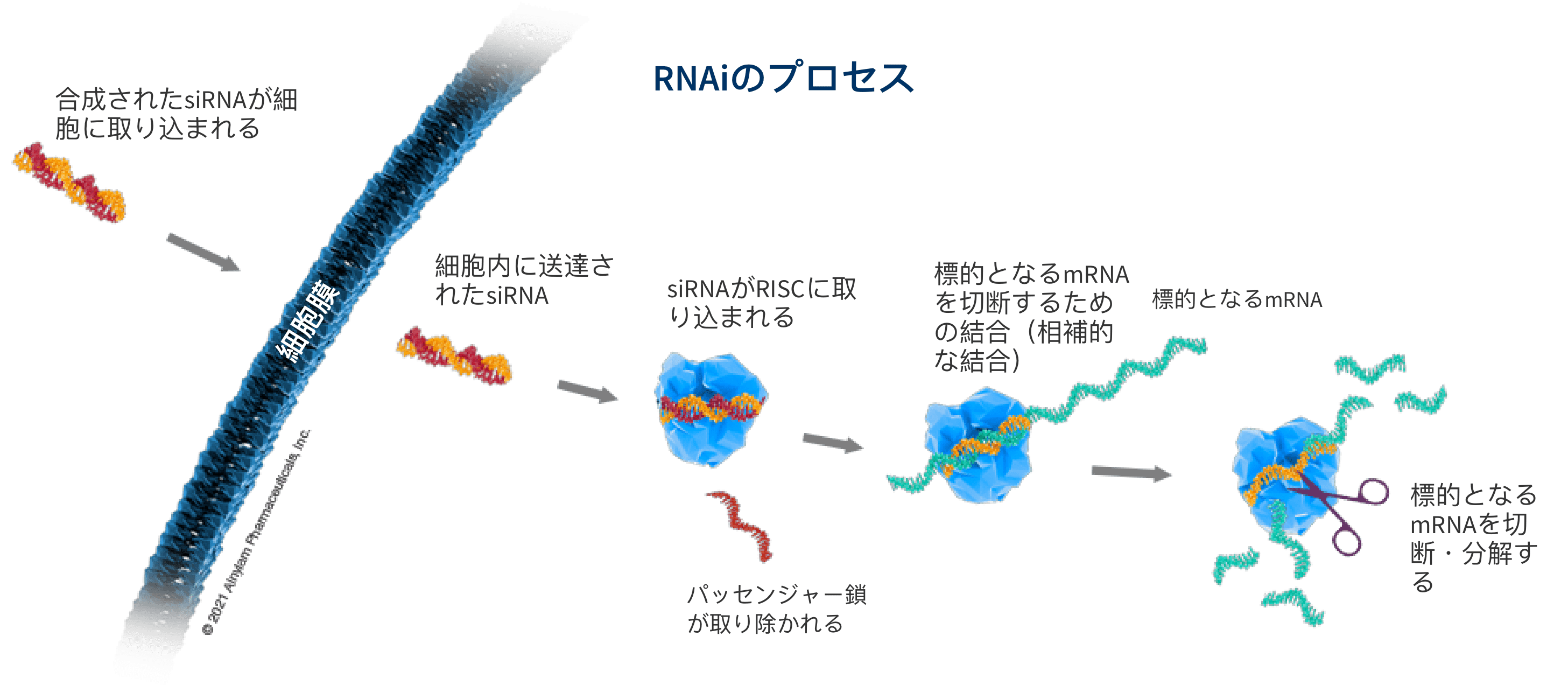
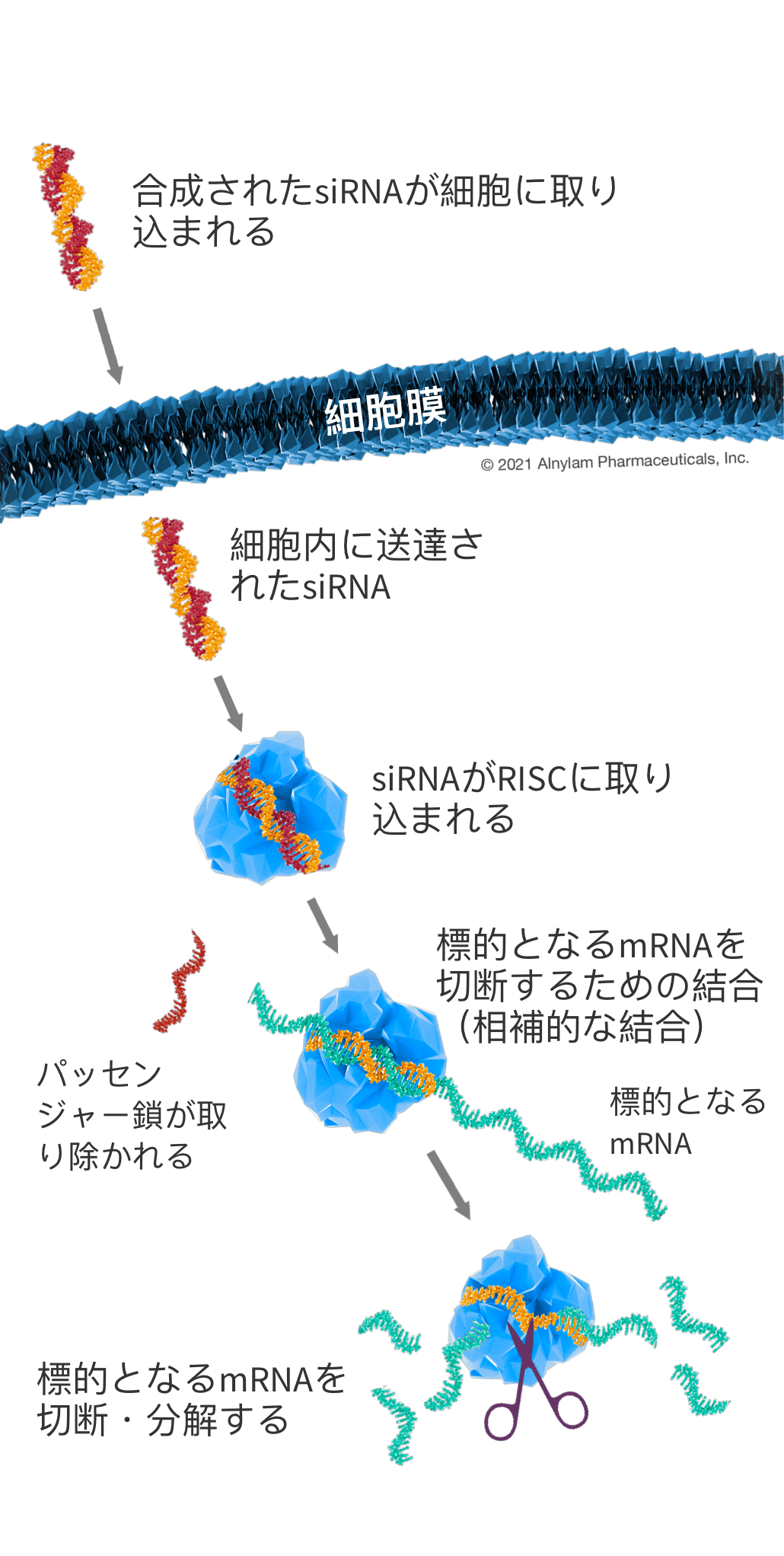
siRNAの仕組み
⼆本鎖siRNAが細胞に送達されると、RNAi経路の主要な構成要素として細胞内に存在するRNA誘導サイレンシング複合体(RISC)と 呼ばれるタンパク質複合体がそれを認識します。RISCに認識されたsiRNAは、⼆本鎖のうちの1つ(パッセンジャー鎖)が取り除 かれます。残されたもう1つの鎖(ガイド鎖)はRISCと結合し、さらに相補的mRNAと結合するのを誘導し、リボソームによってタンパク質に変換される前に、ハサミのように、 “不要” な標的mRNAを切断し、分解させます。このプロセスは 触媒的であり、つまり1本のsiRNAを取り込んだRISCが、多くの標的mRNAを繰り返し分解することができます。それにより、 “不要” なタンパク質の⽣成が減少・抑制されます。
さらに、RNAウイルスやその宿主因⼦を直接標的として破壊し、ウイルスの複製を阻⽌したり、細胞内に侵⼊できないようにし たりするなど、感染症に対応するsiRNAの開発も可能であると考えています。
私たちのRNAi治療薬の主な特徴
- 理論上、低分⼦化合物や抗体では「治療不可能な(undruggable)」標的を含め、ゲノム上のあらゆる遺 伝⼦を標的とすることが可能
- ⾼い有効性と持続的な効果(年2回または年1回という投与頻度の少なさ)を持つ
- 静脈内投与、⽪下投与、吸⼊投与など複数の投与⽅法ができる
- 遺伝⼦を抑制する他のアプローチと⽐較して、低⽤量・低投与頻度でも臨床的有⽤性が実証されており、全体的な安全性も期待できる
- モジュール化されており、再現性が⾼く、どの臓器や疾患においても⼀貫した性能を発揮する









